Reaksi Redoks
I. Reaksi RedoksDi kelas X sudah dibahas mengenai pengertian reaksi redoks. Reaksi redoks adalah reaksi reduksi dan oksidasi. Reaksi reduksi adalah reaksi penangkapan elektron atau reaksi terjadinya penurunan bilangan oksidasi. Sedangkan reaksi oksidasi adalah reaksi pelepasan elektron atau reaksi terjadinya kenaikan bilangan oksidasi. Contoh reaksi redoks dalam kehidupan sehari-hari adalah reaksi perkaratan besi dan pengisian aki pada kendaraan bermotor.
4 Fe + 3 O2 ⎯⎯→ 2 Fe2O3
bo Fe = 0 bo O = nol bo Fe = +3, bo O = –2
Jadi, reaksi redoks adalah reaksi penerimaan dan pelepasan elektron (adanya transfer elektron), atau reaksi redoks adalah reaksi terjadinya penurunan dan kenaikan bilangan oksidasi (adanya perubahan biloks).
contoh ;
1. Manakah yang termasuk reaksi redoks:
A. NaOH + HCl –> NaCI + H2O
B. Ag+(aq) + Cl–(aq) —> AgCl(s)
C. CaCO3 —> CaO + CO2
D. CuO + CO —> Cu + CO2
E. NH3 + H2O —> NH4OH
Jawab: D
Perhatikan atom Cu dari biloks +2 (pada CuO) berubah menjadi nol (pada Cu). Jika satu atom mengalami perubahan biloks, maka pasti akan diikuti oleh perubahan biloks unsur yang lain.
Penyetaraan Persamaan Reaksi Redoks
Cara penyetaraan persamaan reaksi redoks dapat dilakukan dengan dua cara, yaitu cara setengah reaksi dan cara perubahan bilangan oksidasi.
1. Cara Setengah Reaksi
Cara penyetaraan persamaan reaksi redoks dengan cara setengah reaksi, yaitu dengan melihat elektron yang diterima atau dilepaskan. Penyetaraan dilakukan dengan menyamakan jumlah elektronnya. Cara ini diutamakan untuk reaksi dengan suasana reaksi telah diketahui. Cara penyetaraan:
Tahap 1 : Tuliskan setengah reaksi untuk kedua zat yang akan direaksikan.
Tahap 2 : Setarakan unsur yang mengalami perubahan biloks.
Tahap 3 : Tambahkan satu molekul H2O pada:
- Suasana asam: pada yang kekurangan atom O.
- Suasana basa: pada yang kelebihan atom O.
Tahap 4 : Setarakan atom hidrogen dengan cara:
- Suasana asam: dengan menambahkan ion H+.
- Suasana basa: dengan menambahkan ion OH–.
Tahap 5 : Setarakan muatan dengan menambahkan elektron.
Tahap 6 : Samakan jumlah elektron yang diterima dengan yang dilepaskan, kemudian jumlahkan.
Cara Perubahan Bilangan Oksidasi
Cara penyetaraan persamaan reaksi dengan cara perubahan bilangan oksidasi, yaitu dengan cara melihat perubahan bilangan oksidasinya. Penyetaraan dilakukan dengan menyamakan perubahan bilangan oksidasi. Pada cara ini suasana reaksi tidak begitu mempengaruhi, meskipun suasana reaksi belum diketahui, penyetaraan dapat dilakukan.
Tahap 1 : Setarakan unsur yang mengalami perubahan biloks.
Tahap 2 : Tentukan biloks masing-masing unsur yang mengalami perubahan biloks.
Tahap 3 : Tentukan perubahan biloks.
Tahap 4 : Samakan kedua perubahan biloks.
Tahap 5 : Tentukan jumlah muatan di ruas kiri dan di ruas kanan.
Tahap 6 : Setarakan muatan dengan cara:
- Jika muatan di sebelah kiri lebih negatif, maka ditambahkan ion H+. Ini berarti reaksi dengan suasana asam.
- Jika muatan di sebelah kiri lebih positif, maka ditambahkan ion –OH. Ini berarti reaksi dengan suasana basa.
Tahap 7 : Setarakan hidrogen dengan menambahkan H2O.
Reaksi Redoks adalah reaksi yang didalamnya terjadi perpindahan elektron secara berurutan dari satu spesies kimia ke spesies kimia lainnya, yang sesungguhnya terdiri atas dua reaksi yang berbeda, yaitu oksidasi (kehilangan elektron) dan reduksi (memperoleh elektron). Reaksi ini merupakan pasangan, sebab elektron yang hilang pada reaksi oksidasi sama dengan elektron yang diperoleh pada reaksi reduksi. Masing-masing reaksi (oksidasi dan reduksi) disebut reaksi paruh (setengah reaksi), sebab diperlukan dua setengah reaksi ini untuk membentuk sebuah reaksi dan reaksi keseluruhannya disebut reaksi redoks.


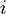 , dilambangkan dengan
, dilambangkan dengan 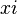 adalah jumlah mol komponen
adalah jumlah mol komponen  adalah
adalah  dan seterusnya. Jumlah fraksi mol dari semua komponen adalah 1. Persamaannya dapat dituli
dan seterusnya. Jumlah fraksi mol dari semua komponen adalah 1. Persamaannya dapat dituli

 P0 - P
P0 - P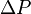 = P0 x Xt
= P0 x Xt )
)
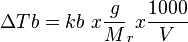

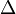 Tb = kenaikan titik didih
Tb = kenaikan titik didih



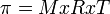
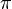 = tekanan osmotik
= tekanan osmotik

